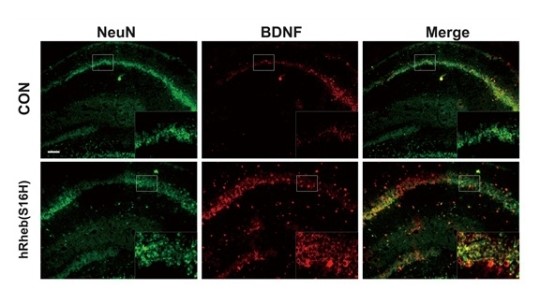
그림 1. 쥐의 해마신경세포에서 Rheb(S16H) 도입에 의한 BDNF 증가 <br>(위) 정상 쥐의 해마신경세포(NeuN 항체로 조직 염색된 부위)에서 BDNF(신경영양인자) 발현 정도에 비해 (아래) Rheb(S16H)가 도입된 신경세포에서 더 많은 BDNF를 발현하고 있다. 이것은 해마신경세포에서 Rheb(S16H)의 발현이 신경영양인자 생산을 유도할 수 있다는 것을 보여준다. 각 그림의 오른쪽 아래 부분은 흰색 사각형 부위를 확대한 그림이다.
경북대 김상룡 교수와 경희대 진병관 교수 연구팀이 기억에 중요한 역할을 담당하는 해마 신경세포를 보호할 수 있는 유전자 구조체(벡터)를 제작했다고 22일 밝혔다. 이는 노인성 뇌질환 관련 신경퇴화 저지를 위한 실마리가 될 것으로 기대된다.

유전자 구조체란 하나의 생물에서 다른 생물에 특정 유전자를 전달하기 위해 유전자를 운반할 수 있는 자율적 증식능력을 지닌 DNA 분자를 뜻한다.
그동안 의료과학계는 고령화에 따라 알츠하이머병과 같은 치매와 파킨슨병 환자가 급속히 증가함에도 불구하고, 신경세포가 점차 손상되는 신경퇴화라는 노인성 뇌질환의 공통적인 병리현상의 원인을 명확히 규명하지 못하고 있다.
따라서 지금은 신경퇴화를 저지하거나 퇴화로 소실된 뇌기능 회복은 어렵고, 다만 증상완화를 위한 치료에 머무르고 있다.
연구팀이 개발한 신경 독성물질로부터 해마 신경세포를 보호할 수 있는 유전자 구조체에는 신경세포의 생존과 성장에 중요한 단백질(mTORC1)의 활성을 유도하는 단백질(Rheb(S16H))에 대한 정보가 들어있어 결과적으로 신경세포 보호효과를 갖는다. Rheb는 신경세포의 분화 및 성장, 생존에 중요한 단백질이다.
실제 신경독성 물질에 노출된 쥐에 유전자 구조체를 주입한 결과, 해마신경세포의 사멸이 현저히 감소했다고 연구팀은 설명했다.
김상룡 교수는 "이번 연구결과는 노인성 뇌질환과 연관될 수 있는 성체신경세포의 활성과 보호를 위해 어떤 타깃을 고려해야 될 지 중요한 단서를 제공하는 것"이라고 말했다.
이번 연구성과는 생명공학 및 응용미생물학 분야의 권위지이자 네이처의 자매지인 몰레큘러테라피(Molecular Therapy) 13일자 온라인판에 게재됐다.
류준영 기자 joon@mt.co.kr
머니투데이

 유전자 구조체란 하나의 생물에서 다른 생물에 특정 유전자를 전달하기 위해 유전자를 운반할 수 있는 자율적 증식능력을 지닌 DNA 분자를 뜻한다.
유전자 구조체란 하나의 생물에서 다른 생물에 특정 유전자를 전달하기 위해 유전자를 운반할 수 있는 자율적 증식능력을 지닌 DNA 분자를 뜻한다.  朝鲜语字母挂图
朝鲜语字母挂图 성공한 사람들의 시간관리습관--成功人士的时间管理方法
성공한 사람들의 시간관리습관--成功人士的时间管理方法 두 대양의 비밀--两个海洋的秘密(朝鲜文)
두 대양의 비밀--两个海洋的秘密(朝鲜文) 흔히보는 질병과 식이료법/常见病及其饮食疗法
흔히보는 질병과 식이료법/常见病及其饮食疗法 올리버 트위스트--雾都孤儿(朝鲜文)
올리버 트위스트--雾都孤儿(朝鲜文) 80일간의 세계일주--八十天环游地球(朝鲜文)
80일간의 세계일주--八十天环游地球(朝鲜文)